外观
外观
约 1048 字大约 3 分钟
2026-03-06
我们引入一些可以观测的量:体膨胀系数、压强系数和等温压缩系数,
α=V1(∂T∂V)p,β=p1(∂T∂p)V,κT=−V1(∂p∂V)T
小结一下利用热力学定律研究均匀系统性质的一般方法:
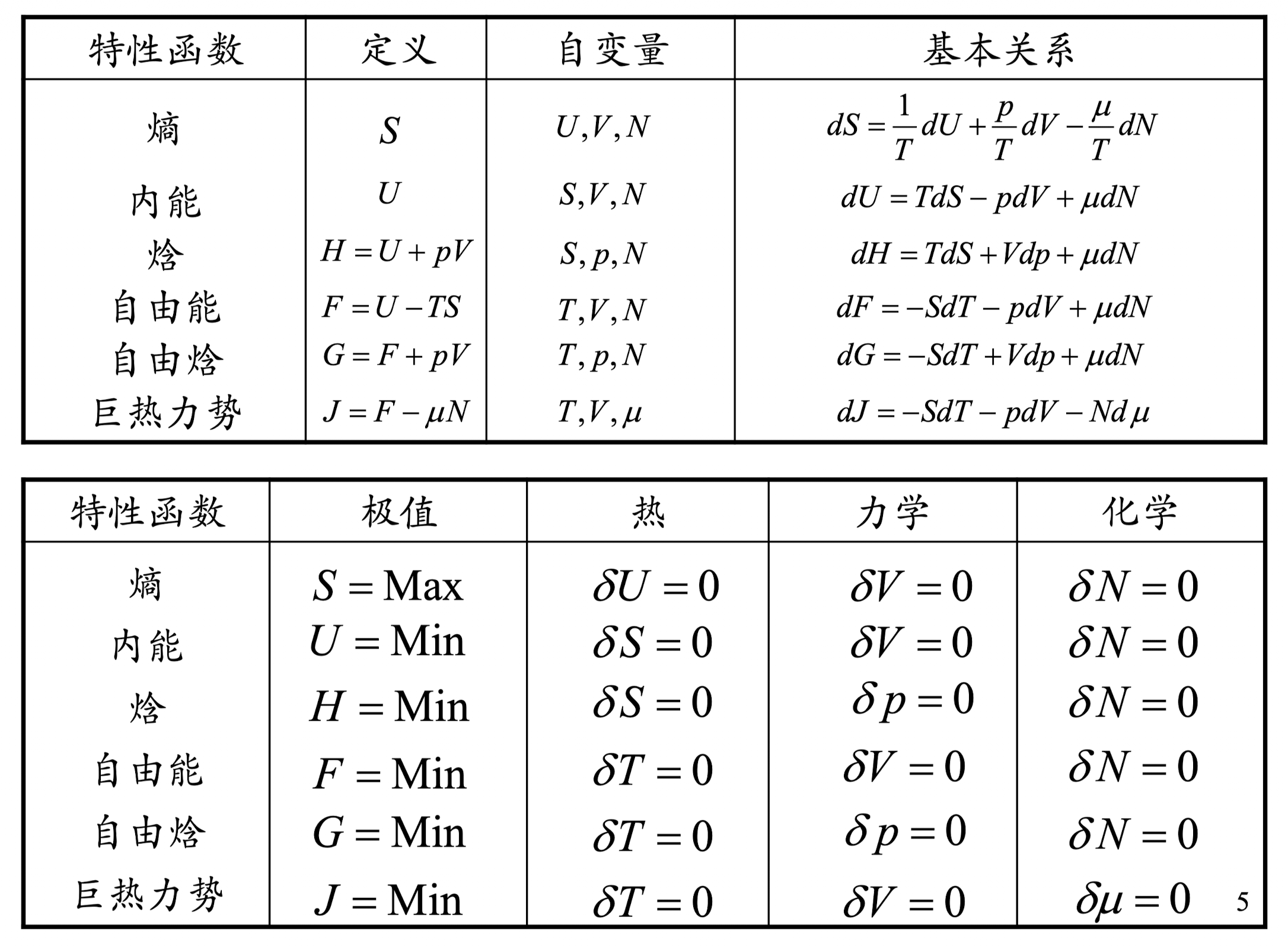
平衡态的特性函数:

从 Nernst 定理 (1906) 开始,Nernst 定理指的是等温过程中熵的改变在 T→0 下趋于零,即
T→0lim(ΔS)T=0
1912 年,Nernst 提出 Nernst 原理,表述为:不可能使一个物体冷却到绝对温度的零度.
如果考虑热容
Cy=T(∂T∂S)y
在没有受力的情况下,能够从初始值开始计算熵的具体值,
S(T,y)=S(0,y)+∫0yCyTdT
我们可以把 S(0,y) 设为 0,这是 Planck 的做法. 同时根据 Nernst 原理可以证明,在 T→0 时比热必须趋于零,否则和 Nernst 原理 (或者说热力学第三定律) 矛盾.
现在要考虑粒子数可变系统,设均匀系有 k 个组元,以 T,p,{Ni} 为自变量,对于 G 这种广延量,有
G=i=1∑kNi(∂Ni∂G)T,p,Nj=Ni=i∑Niμi
这里用到所谓 Euler 定理:如果齐次函数
f(λx1,⋯,λxn)=λmf(x1,⋯,xn)
则
I∑xi∂xi∂f=mf
这里定义了第 i 组元的化学势 μi. 新的热力学方程是
dG=(∂T∂G)p,NidT+(∂p∂G)T,Nidp+i∑(∂Ni∂G)T,p,Nj=NidNi
和封闭系统比较,上式可以用特性函数表示为
dG=−SdT+Vdp+i∑μidNi
可以定义 mol Gibbs 函数:
G(T,p,n)=nGm(T,p),Gm=(∂n∂G)T,p≡μm≡NAμ
用孤立系统来讨论,考虑两相 α,β. 要求能量、体积、粒子数都恒定,也就有
Uα+Uβ=const.,Vα+Vβ=const.,Nα+Nβ=const.
平衡时,S 取极值,δS=δSα+δSβ=0. 也就是:
⟹TαδUα+pαδVα−μαδNα+TβδUβ+pβδVβ−μβδNβ=0(Tα1−Tβ1)δUα+(Tαpα−Tβpβ)δVα+(Tαμα−Tβμβ)δNα=0
有三个平衡条件,热平衡条件 Tα=Tβ、力学平衡条件 pα=pβ、相平衡条件 μα=μβ.
对于多元复相系,平衡条件也是上面这些. 如果存在化学反应则更复杂:以 2H2+O2⟷2H2O 为例,热力学习惯于写成
2H2O−2H2−O2=0
一般地,写为
i=1∑kνiAi=0
等温等压条件下,Gibbs 自由能极小,δG=0. 化学平衡条件和化学反应的系数有关,
i∑νiμi=0
用宏观量来描写相变,首先是 Gibbs 相律,描述相的并存:
μI(T,Y)=μII(T,Y)⟹Y=Y(T)
这个 Y(T) 称为两相共存曲线. 如果是三相共存,则可以解出一个点,这个点三相共存,称为三相点. 同理可以知道四相一般不能共存.
cfd28-feat(note): update bote于